Menu
Entrar
Es una enfermedad donde el Pulmón es dañado de manera crónica, repetitiva o de forma muy intensa, lo que causa una acumulación de tejido fibrótico similar a las cicatrices, que engrosan y hacen más rígido el tejido funcional pulmonar, causando alteraciones irreversibles en la oxigenación y que su empeoramiento produce mayor dificultad respiratoria.
Afecta generalmente a personas mayores de 50 años de edad.
La mayor parte de las veces no se puede saber con certeza la causa de la enfermedad, pero se ha asociado a:
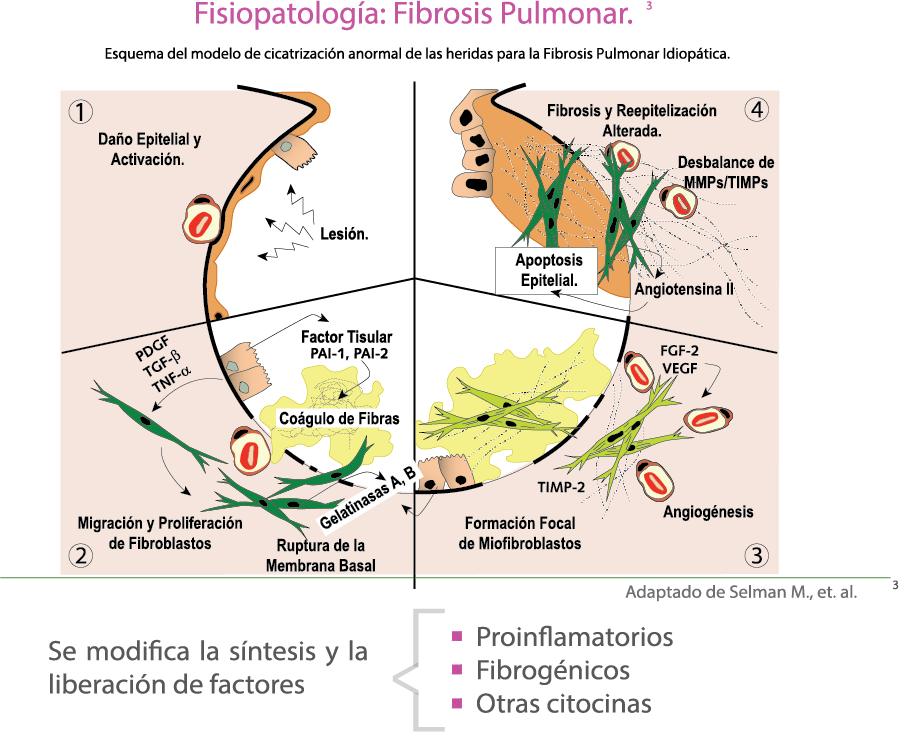
La Fibrosis es precedida y provocada por una inflamación crónica, por daño al pulmón, que altera la fibrogénesis, dejando al final cicatrices fibróticas.

La Pirfenidona:
KitosCell-LP® es un potente inhibidor del Factor de Necrosis Tumoral Alfa (TNF-α) y controla la respuesta inflamatoria:
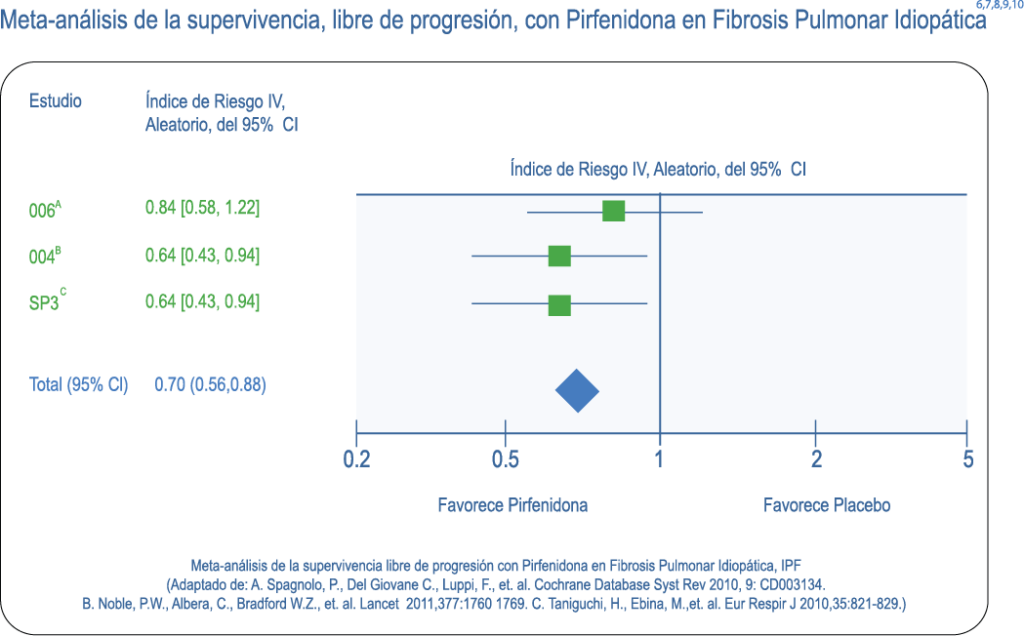
Revisión: Agentes no esteroides para Fibrosis Pulmonar Idiopática.
Comparación: Pirfenidona vs placebo.
Variable: Cambio basal absoluto de la capacidad vital.

Pirfenidona reduce la progresión en la disminución de la capacidad vital y la capacidad vital forzada.
De todos los medicamentos estudiados para el tratamiento de la Fibrosis Pulmonar Idiopática, la Pirfenidona es la que tiene el mayor grado de evidencia para soportar su eficacia y es el primer medicamento aprobado para el uso de esta indicación.
Los resultados mostraron que después de un año, la adición de pirfenidona, prednisona y azatioprina se asoció con mejora, en comparación con el tratamiento inmunosupresor solo con prednisona y azatioprina. Entre los puntos finales de eficacia preestablecidos la adición de pirfenidona dio lugar a una tendencia marginal a la mejora en el intercambio de gas (DLCO), una mejora significativa en la calidad de vida de acuerdo con la puntuación total en el SGRQ, con tendencia a ser significativa en VAS.
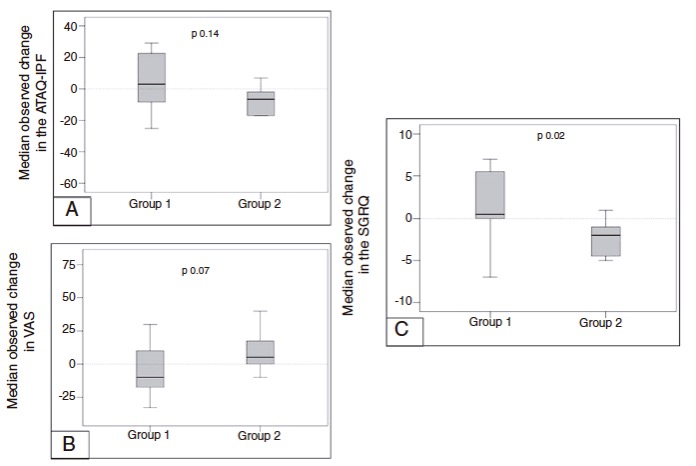
El cambio medio en los cuestionarios de calidad de vida en las puntuaciones en ambos grupos desde el inicio hasta los 12 meses de tratamiento. [A] Puntuación ATAQ-IPF, [B] Puntuación VAS y [C] Puntuación SGRQ. Grupo 1 (Prednisona y Azatioprina), Grupo 2 (Prednisona, Azatioprina y Pirfenidona)
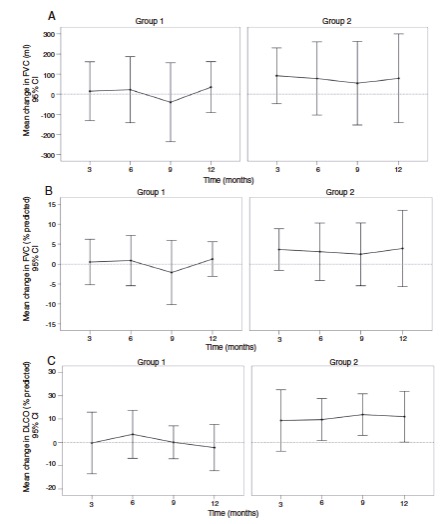
Cambios en las pruebas de función respiratoria, Grupo 1 (Prednisona y Azatioprina), Grupo 2 (Prednisona, Azatioprina y Pirfenidona)
Eficaz en Fibrosis Pulmonar.
Sistema de liberación prolongada de fácil dosificación y con mínimos efectos secundarios.
Mejora el pronóstico de sobrevida del paciente.
Vía de administración: Oral.
Adultos: 1200 mg a 2400 mg al día, dividido en dosis cada 12 horas.
Niños mayores de 12 años: 600 mg – 1200 mg al día, dividido en dosis cada 12 horas.
Para prescripción por Médico Especialista.
Por superficie corporal: 250 mg – 500 mg/dosis por m2 de superficie corporal.
En pacientes con Insuficiencia Hepática Severa, se recomienda efectuar un monitoreo de aminotransferasas y deberá ajustarse la dosis de acuerdo a los valores del estudio.
Caja con 90 Tabletas de Liberación Prolongada de 600 mg.
La tableta puede ser fraccionada, cuando así se requiera, con base en la dosificación recomendada.
Preferentemente, ingerir a los 20 a 30 minutos después de los alimentos.
1. Azuma, A. (2012) Pirfenidone treatment of idiopathic pulmonary fibrosis. Ther Adv Respir Dis 6(2) 107-114.
2. Selman, M., Thannickal, V.J., Pardo, A., Zisman, D.A. Martinez, F.J., Lynch III. (2004) Idiopathic Pulmonary Fibrosis Pathogenesis and Therapeutic Approaches (Review Article) Drugs 2004; 64 (4): 405-430.
3. Selman, M., Talmadge,E., King, Jr., Pardo, A. (2001) Idiopathic Pulmonary Fibrosis: Prevailing and Evolving Hypotheses about Its Pathogenesis and Implications for Therapy. Ann Intern Med. 2001; 134: 136-151
4. Taniguchi, H., Kondoh, Y., Ebina, M., Azuma, A., Ogura, T., Taguchi, Y., Suga, M., Takahashi, H., Nakata, K., Sato, A., Sugiyama, Y., Kudoh, S., Nukiwa, T., (2011). The Clinical Significance of 5% change in vital capacity in patients with idiopathic pulmonary fibrosis: extended analysis of pirfenidone trial. Respiratory Research 2011, 12:93
5. Adalami, H., Maher, T.M. (2012) Current and novel drug therapies for idiopathic pulmonary fibrosis. Drug Design, Development and Therapy 2012; 6 261-272.
6. Spagnolo, P., Del Giovane, C., Luppi, F., Cerri, S., Balduzzi, S., Walters, E.H. (2010) Non-steroid agents for idiopathic pulmonary fibrosis. Cochrane Database Syst Rev 9: CD003134
7. Noble, P.W., Albera, C., Bradford W.Z., et al., (2011) Pirfenidone in patients with idiopathic pulmonary fibrosis (CAPACITY): two randomized trials. Lancet 2011; 377: 1760-1769.
8. Taniguchi, H., Ebina, M., Kondoh, Y., Ogura, T., Azuma, A., Suga, M., Taguchi, Y., Takahashi, H., Nakata, K., Sato, A., Takeuchi, M., Raghu, G., Kudoh, S., Nukiwa, T., (2010). Pirfenidone in idiopathic pulmonary fibrosis. Eur Respir J 2010; 35: 821-829.
9. Albera, C., Ferrero, C., Rindone, E., Zanotto, S., Rizza, E. (2013) Where do we stand with IPF treatment? Respiratory Research 2013 14 (Suppl 1): S7, 1-3
10. Behr, J. (2013) Evidence-Based treatment strategies in idiopathic pulmonary fibrosis. Respiratory Research 2013, 14 (Suppl 1): S7
11. Richeldi, L. (2013) Clinic trials of investigational agents for IPF: a review of Cochrane report. Respiratory Research 2013, 14 (Suppl 1): S4